Improve Health
近日,领星医学联合复旦大学附属中山医院周宇红教授团队开展了一项回顾性研究,该研究探索了 TKIs 联合 ICIs 在不同肉瘤亚型中的疗效,这是至今为止国内最大样本量的有关肉瘤免疫治疗的回顾性研究,为软组织肉瘤患者提供了新的治疗策略。相关成果「Activity of PD-1 Inhibitor Combined With Anti-Angiogenic Therapy in Advanced Sarcoma: A Single-Center Retrospective Analysis」发表于「Frontiers in molecular biosciences (IF:5.246)」。复旦大学附属中山医院游洋博士为本研究的第一作者,领星完成 NGS 测序及分子标志物的筛选 。
软组织肉瘤(STS)是一种罕见的癌症,约占成人恶性肿瘤的 1%,由 100 多种不同的亚型组成。近年来,免疫检查点抑制剂(ICIs)单药在肉瘤的探索均表明患者疗效欠佳,仅少于 20% 的患者能从中获益。
令人欣喜的是,抗 VEGF 受体酪氨酸激酶抑制剂(TKIs)联合治疗在腺泡状软组织肉瘤(ASPS)显示出一定的抗肿瘤活性。然而,这一疗法在脂肪肉瘤(LPS)、平滑肌肉瘤(LMS)、粘液纤维肉瘤(MFS)等其它亚型中的疗效尚缺乏广泛研究。

主要发现
本研究回顾性分析了 61 例晚期 STS 患者的临床数据,旨在探索免疫联合治疗在不同肉瘤亚型中的疗效和有效预测患者预后的生物标记物。研究发现,经 ICIs 联合 TKIs 治疗后,患者中位 PFS(mPFS)显著延长(HR 0.5464,p = 0.043);患者 12 个月的 PFS 率从 20.26% 提高至 42.9%。
研究结果
1. 患者基线特征
研究纳入 61 例 STS 患者,其中 41 例接受 ICIs+TKIs 治疗,20 例接受 ICIs 单药治疗。两组(ICIs+TKIs vs ICIs)患者基线无显著差异(表 1)。大多数患者在免疫治疗前接受了化疗和平均 2 个周期的传统治疗。

▲ 表 1 患者基线数据分析
(注:PR partial response; CR complete response; SD stable disease; PD progressive disease)
2. 疗效
研究发现 ICIs+TKIs 组有 12 例患者达到 PR,25 例 SD,3 例 PD。而 ICIs 单药组仅有 2 例患者达到 PR,14 例 SD,5 例 PD。两组的 ORR 分别为 9.5% 和 30%。1 例 DDLPS 患者达到了 pCR,没有患者达到 CR。
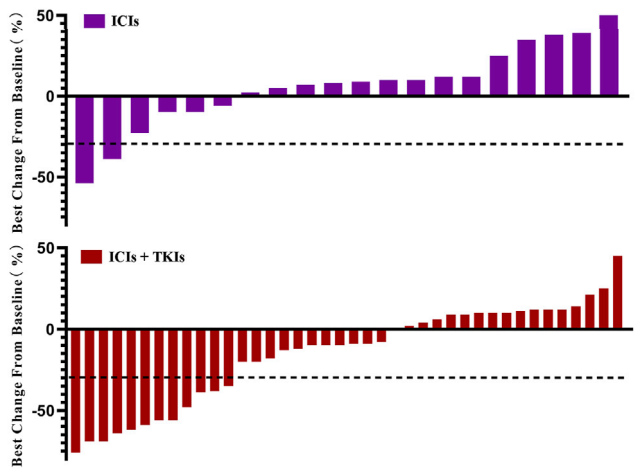
▲ 图 1 患者肿瘤负荷变化(ICIs+TKIs, n = 40; ICIs, n = 20)
相比 ICIs 单药治疗,联合治疗提高了 ORR 和 DCR(CR+PR+SD)(ORR 10 vs 31.7%; DCR 80 vs 87.9%)。其中 UPS、ASPS 和 MFS 患者响应率最高,LMS 亚型响应较差。

▲ 图 2 不同肉瘤亚型临床响应情况:(A)两组肿瘤负荷变化(相比基线)(B)不同亚型肿瘤负荷变化
通过对两组患者无疾病生存期分析显示,ICIs+TKIs 组相比 ICIs 组 mPFS 显著延长(11.74 个月 vs 6.81 个月; HR 0.55, 95% CI 0.2673–0.9791, p = 0.043)。

▲ 图 3 两组 PFS 分析
3. 安全性
研究中发生的治疗相关不良事件主要包括皮疹 (14.8%)、发热 (16.4%)、疲劳 (26.2%)、甲状腺功能减退 (18%)、高血压 (50.8%)、ALT/AST/ALP 水平升高 (41.0%)、维生素 D 缺乏 (37.7%) 等。两组均未发生 4 级以上不良事件。
研究结论
本研究证实 PD-1 抑制剂联合抗血管生成抑制剂治疗可以提高 STS 患者的 mPFS(5 个月以上)、ORR 和 DCR。此外,亚组分析显示 ASPS 和 MFS 患者对免疫联合治疗更敏感。
作者简介
周宇红 教授 主任医师
◆复旦大学附属中山医院肿瘤内科副主任
◆复旦大学附属中山医院生物治疗中心主任
◆中国抗癌协会肉瘤专业委员会放化疗学组副组长
◆CSCO 肉瘤专业委员会常委
◆上海市抗癌协会肉瘤专业委员会副主任委员
◆中国研究型医院学会腹膜后与盆底疾病专委会常委
◆中国医师协会肛肠医师分会腹膜后疾病专委会副主任委员
◆上海医学会肿瘤学分会骨软肿瘤学组秘书
参考文献:
1.You Y, Guo X, Zhuang R, et al. Activity of PD1 inhibitor combined with anti-angiogenic therapy in advanced sarcoma: a single-center retrospective analysis. Frontiers in Molecular Biosciences, 2021.8.994.
2.D’Angelo SP, Mahoney MR, Van Tine BA. A Non-comparative Multi-center Randomized Phase II Study of Nivolumab +/− Ipilimumab for Patients with Metastatic Sarcoma (Alliance A091401). Lancet Oncol. 2018.19, 416–426.
3.Judson I, Verweij J, Gelderblom H. Doxorubicin Alone versus Intensified Doxorubicin Plus Ifosfamide for First-Line Treatment of Advanced or Metastatic Soft-Tissue Sarcoma: a Randomised Controlled Phase 3 Trial. Lancet Oncol. 2014.15, 415–423.
4.Tawbi HA, Burgess M, Bolejack V. Pembrolizumab in Advanced Soft-Tissue Sarcoma and Bone Sarcoma (SARC028): a Multicentre, Two-Cohort, Single-Arm, Open-Label, Phase 2 Trial. Lancet Oncol. 2017.18, 1493–1501.
5.Wilky BA, Trucco MM, Subhawong TK. Axitinib Plus Pembrolizumab in Patients with Advanced Sarcomas Including Alveolar Soft-Part Sarcoma: a single-centre, Single-Arm, Phase 2 Trial. Lancet Oncol. 2019.20, 837–848.
图片来源:领星
Improve Health