案例简介:该案例是一例选用索拉菲尼做术后辅助治疗的具有挑战性的案例。为最大限度地达到 R0 切除的效果并同时保证患者术后肝脏体积的恢复,手术设计为右半肝联合右侧尾状叶的切除。截至目前,患者术后一年仍维持未复发的状态。
病史资料
患者男性,57 岁,体检发现肝内实性占位 10 日余,2018-03-06 入我院治疗,自述既往 50 年乙肝病史, 入院体格检查无异常。
实验室检查:
· CA19-9 114.60 U/mL
· HBsAg(+),HBsAb(-),HBcAb(+),HBeAb(+),HBeAg(-)
· HBV-DNA 定量<500 IU/ml
· ICG R15:9.20%
· 其他生化指标正常,血常规、凝血指标正常
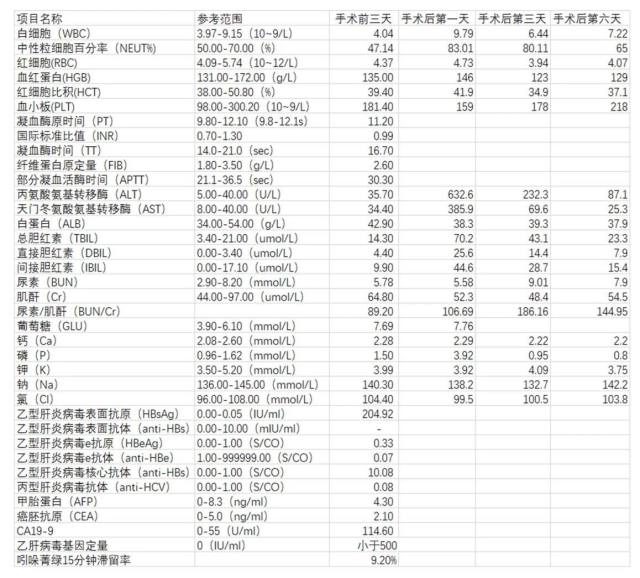
图 1 患者实验室检查结果
肝脏增强 MRI:
在 T2 像可以看到一枚位于尾状叶腔静脉旁部的实性结节,边界欠清。注入特异性对比剂后,可以看到动脉期肿瘤边缘强化,门脉期、延迟期,信号缓慢减低。在门脉期可以看到肿瘤的外周被门脉右支及门脉右后支包绕。延迟期肿瘤外周呈晕环状,结合患者的乙肝病史,给予患者诊断为肝占位(肝细胞癌可能性大)(图 2)。
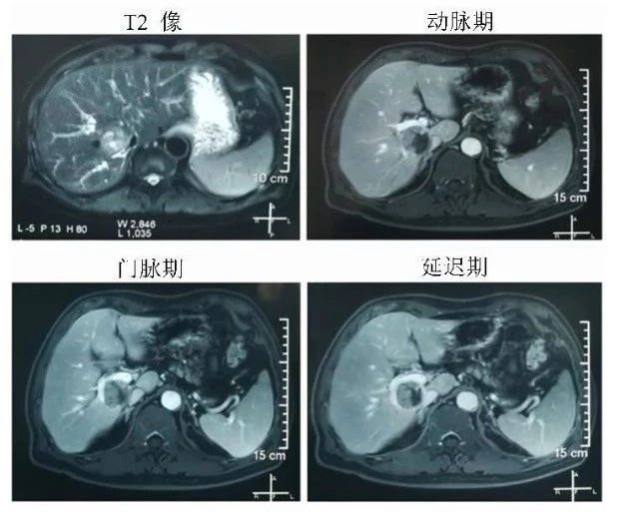
图 2 患者肝脏增强 MRI 影像学评价
治疗方案
结合 2017 版原发性肝癌诊疗规范(2017 版)对患者进行评估:
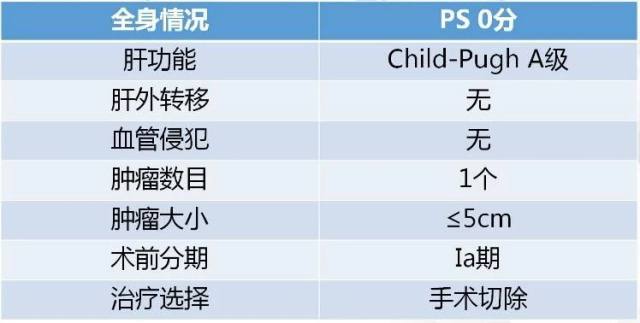
图 3 患者术前评估
Q:切除范围应选择单纯的尾状叶切除还是联合右半肝的尾状叶切除呢?
首先患者的胆红素水平处于正常范围,吲哚青绿 15 分钟滞留率<10%,左半肝的剩余肝脏体积为 46.3%,完全可以耐受右半肝切除。
其次,在位置上,肿瘤被门脉右支和门脉右后支包绕,联合行右半肝切除不仅减低了手术难度,减少了术中对肿瘤的挤压,这种联合右半肝切除方式对于这名患者的愈后可能有更大的益处。
手术方案:
2018-03-09 保留尾状叶的固有部,选择了右半肝联合右侧尾状叶的切除。
术后病理:
·(肝脏)中分化肝细胞癌
· Edmonson-Steiner 分级:Ⅱ级
· 肿瘤边界欠清,肿物距切缘最近约 0.4 cm
· MVI 评分 = M1
· 卫星结节一枚
免疫组化结果:
Glypican-3 (+) , CEA (-) , CK8-18 (+) , CK19 (胆管+) , HBSAg (+) , Hepatocyte (部分细胞+) , P53 (-) , Ki67 (+20%) , D2-40 (脉管+) , EGFR (+) , VEGF (+) , PD-1 (-) , PD-L1 (-) , CD34 (血管+) , AFP (-) , CD10 (+) 。
患者的肿瘤为中分化肝细胞癌,肿瘤外周发现一枚直径 1.5 cm 的卫星结节,患者 MVI 评分为 M1,手术最近切缘距离为 0.4 cm,这些高危复发风险因素提示了进一步治疗的必要性。
免疫组化的结果显示,肿瘤组织的 VGFR、EGFR 和 CD-34 的结果是阳性, 提示肿瘤的促血管生成活性比较强;Ki67 的结果提示, 肿瘤的增殖能力比较强。
此外,肉眼下切除只能达到解剖学的根治,很难达到肿瘤学的根治。
以上几点均提示了对患者进行辅助治疗的必要性。
Q:术后的辅助治疗应选择哪种方案?
介入治疗:该患者缺乏可靠的可供栓塞的血管。
放疗:2009 年首尔大学对于肝细胞癌切除术后辅助放疗的患者肝脏组织恢复的回顾性分析显示,接受术后辅助放疗的患者在术后 12 周内肝脏组织的恢复情况要远慢于没有进行辅助放疗的患者,尤以 4-12 周最为显著。
药物治疗:由于患者家属表示对患者后续的生活质量要求较高,而化疗对于肝癌的治疗虽有一定的效果,但副反应较大,因而也未考虑对该患者进行化疗。最终,选择为患者进行靶向治疗。
Q:靶向治疗该如何选择?
基于肿瘤组织的全外显子测序
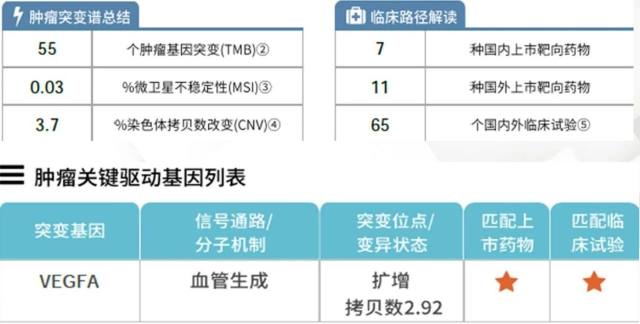
图 4 基于肿瘤组织的全外显子测序结果
免疫治疗:该患者的肿瘤突变负荷为 55。根据大样本回顾分析显示,肝癌患者的突变负荷的三分位数为 167,而该患者属于突变负荷较低的类型;微卫星不稳定的比例为 0.03%,低于参考值 3.5%。此外,免疫组化 PD-1,PD-L1 均为阴性。以上结果均提示患者通过免疫治疗获益的可能性较低。
靶向治疗:在关于肿瘤突变驱动基因的筛选中,该患者仅有 VEGFA 一个驱动基因发生突变。由于肝切除术后辅助治疗相较于进展期肝癌的药物选择还是有一定的差异的,在术后辅助治疗中应该更加重视药物的安全性和患者对药物的耐受性。在患者接受治疗时,仅有索拉菲尼在中国获批上市,并且其对于 VEGFA 突变基因的作用较为确切,最终为患者选择了应用索拉非尼进行辅助治疗。
疗效及预后分析
患者对于索拉非尼的依从性较高,未出现不良反应,术后第 1 个月、第 3 个月复查肝脏体积增加(图 5)。
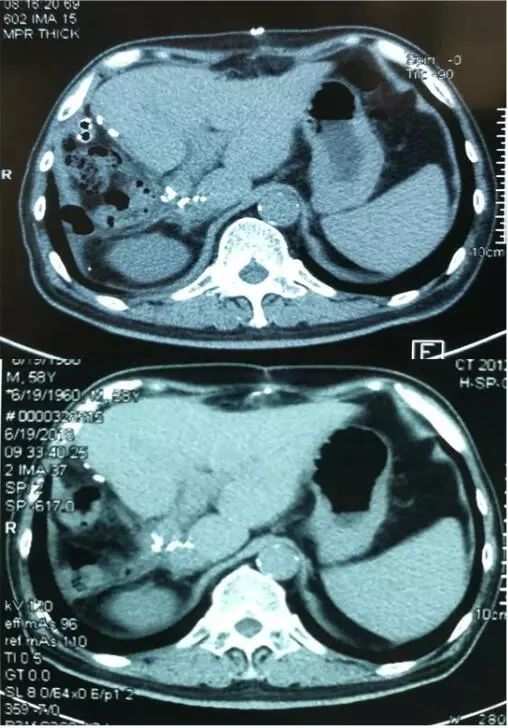
图 5 术后第 1 个月、第三个月肝脏平扫 CT
术后 9 个月复查,实验室检查未见显著异常:
· AFP 3.37 ng/mL
· CEA 3.95 ng/mL
· CA19-9 14.4 U/mL
术后监测的肝胆脾彩超,肺 CT 未见复发迹象。
ctDNA 监测报告显示患者的 ctDNA 呈稳定下降的趋势,在突变基因监测中未发现新的干系基因及耐药基因的出现(图 6)。

图 6 患者外周血 ctDNA 丰度变化曲线
综上,目前该患者一般状态良好,继续口服索拉菲尼 400 mg/次(一日两次),规律口服恩替卡韦,并继续随访。
总结
☆ 肝切除术后高危复发风险人群辅助治疗模式的探索
☆ 肝切除术后高危人群辅助治疗适应症的探索
☆ 多模式治疗手段的联合应用会让患者获得更大的收益
感谢由哈尔滨医科大学附属第一医院周烁医师提供的精彩案例
周烁医师

2017 级哈尔滨医科大学附属第一医院普外科硕士研究生,导师:刘连新教授。
第三届全国大学生基础医学实验设计大赛优秀奖,参与科技部国家重点研究课题一项。
关于领星
领星医学是由中美生物医学科学家携手资深肿瘤专家共同开创的肿瘤精准医疗服务平台,是一家集精准治疗方案筛选、精准治疗实施、精准治疗监测于一体的国际化公司,致力于从信息层面到操作层面集成化的高效服务,为肿瘤患者带来实质临床获益。通过人工智能,医疗大数据的驱动,逐步优化医疗资源的配置,医疗决策的落地,打通整体化,全方位的医疗路径,为中国的肿瘤患者和医生提供个体化精准医疗的临床解决方案及面向全球资源的对接服务。
领星医学检验所是领星医学和北京大学生命科学华东产业研究院联合挂牌的实验室,取得卫计委颁发的医疗机构执业许可,致力于为全国肿瘤患者或医疗机构提供以精准治疗为目的、以基因检测为核心的个体化检验项目与服务。
实验室严格按照ISO15189:2012、美国临床实验室改进修正CLIA'88、美国病理学家协会(CAP)的标准建立了完善的质量管理体系,为美国医疗机构提供临床检验报告的资质,以便有效利用欧美先进医疗技术,更好地为肿瘤患者、医疗机构提供服务。
此外,领星医学还将不断扩充和完善现有数据库,打造集约化的国际化标准检测平台、服务于最先进临床研究的生物信息分析平台和中国最大且符合国际标准的临床数据库,实现产业集群联动,成为具有国际水准的精准医学创新载体。
领星医学始终秉承从精准出发,不断创新,将最新的基因检测技术应用到临床,为临床医生提供专业的分子诊断策略,为更多肿瘤患者带来曙光。
